過去最多の30ヵ国・地域から720社が出展
低分子からバイオまで創薬、開発、製造をサポートする国際医薬品展
(同時開催:ファーマIT / Medtec Japan)
2023年は数年ぶりに世界20カ国以上、約2万人の製薬関係者が来場して医薬品開発のための商談や最新技術の発表が行われました。2023年開催からリブランディングを行ったCPHIは、創薬から製造までをワンストップで提供する医薬品開発展として新薬開発や安定供給をサポート致し、製薬業界の活性化を図るイベントとしてさらなる成長を目指します。
今後、市場成長率の低迷が予想されている日本の製薬業界では、市場の牽引役として新しい抗がん剤の開発が期待されている他、核酸、ペプチド等の中分子を含めたバイオ医薬品の開発、遺伝子医療・細胞医薬やデジタルヘルスなどの新しいモダリティへの取り組みが進んでいます。
本展では、このような業界の課題をサポートするために最適なパートナーの発掘や先端技術を紹介する場として製薬業界の発展、市場の活性化を図ります。
CDMO、核酸・ペプチド医薬品など最新トレンドをテーマとしたプログラムを多数展開
次回開催では、近年の世界的なトレンドともいえるCMO/CDMO、がんや難病の治療薬の開発が期待されているバイオファーマをテーマとしたコンファレンス&展示ゾーンを設置します。
近年、製薬業界では開発期間の長期化に伴い、開発費が年々増大しており、創薬などの研究領域に注力するため、開発・製造部門では、 CMO(医薬品受託製造企業)、CDMO(医薬品受託開発製造企業)等へのアウトソーシングが増加しています。
特にベンチャー企業が多いバイオ医薬品分野では、外部パートナーとの協業は必然であるとも言えます。
本展ではこのような業界ニーズに応えるために、国内外の最新技術動向やノウハウを展示会、コンファレンスを通じてご提供いたします。
CPHI Japan is the leading global community for pharmaceutical professionals in Japan.
Who attends CPHI Japan?
国内で最大級の規模を誇る、医薬品の研究、開発、製造をサポートするイベントとして、毎年春に国内および海外から製薬業界関係者が一堂に集結します。
-
 + 20,000研究、開発、製造、購買部門等を
+ 20,000研究、開発、製造、購買部門等を
中心とした製薬関係者が参加 -
 + 650製薬業界をリードする
+ 650製薬業界をリードする
原料、機器、サービスの
サプライヤー企業が出展 -
 + 200市場、業界動向、最新技術を
+ 200市場、業界動向、最新技術を
業界団体、製薬企業等の
キーパーソンが講演 -
 + 3,000海外の製薬業界関係者が多数来場
+ 3,000海外の製薬業界関係者が多数来場
|
|
CPHI Japan(国際医薬品開発展) テーマゾーン
同時開催イベント
-

ファーマIT&
デジタルヘルスエキスポ -
バイオファーマ
セミナー -

Medtec Japan
-

ジャパン
ライフ
サイエンスウィーク -
創薬イノベーションセミナー
-

セミナープログラム
最新の規制動向、業界の課題から最新トレンドをキーパーソンが概説する他、世界の有力サプライヤーが最新技術を発表。3日間で約200セッションを開催。(全セッション無料)
-


展示会
過去最大規模となる、世界約30ヵ国・地域から約720社が出展。 創薬、開発、製造をサポートするビジネスパートナーと出会う絶好の機会となります。
-

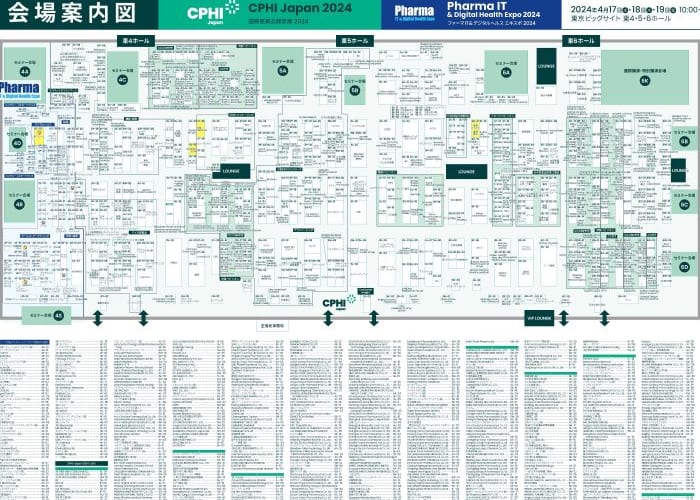
会場案内図
原料、アウトソーシング、バイオ、機器・装置、DDS・パッケージングの5つのテーマゾーンと同時開催のファーマITをカバーした会場MAP。開催前のご来場計画にご活用ください。
-

ビジネスマッチメイキング
会期前に出展社とミーティングやブース訪問のアポイントが取得できるサービスです。WEB来場登録後にご利用が可能です。(無料)
-

パートナーシップ
「ヘルスケア&製薬業界におけるインドと日本間の恒久的なパートナーシップの構築にむけて」をテーマにインド&日本の関係者が特別講演を行います。
-

インド市場への進出
日本の製薬産業がグローバルに展開する中で直面する様々な課題や成功のヒントを共有し、インド市場への戦略的進出について解説します。
-

サステナビリティ企画
CPHIでは世界各国でサスティナビリティの取り組みを推進しています。 本年の開催では経験豊富な講師によるセミナーやネットワーキングを開催します。




































